면역세포치료제 개발에서 유전자 편집 기술의 역할
장미희 한국과학기술연구원 책임연구원
이수민 한국과학기술연구원 박사후연구원
1. 개요
최근 활발히 개발되는 유전자면역세포치료제는 ex vivo 방식으로, 환자 자가 또는 동종 세포를 채취해 생체 외에서 표적 유전자를 도입/조작한 뒤 다시 체내에 투여해 질환을 치료하는 기술로 혁신적 암 치료제로 주목받고 있다.
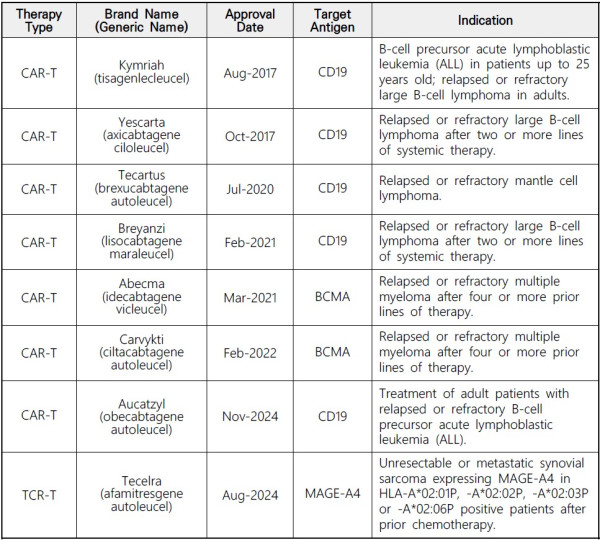
현재까지 유전자가 변형/도입되어 미국 FDA에 승인된 면역세포치료제는 8종으로 백혈병, 림프종, 및 골수종을 표적으로 하는 CAR-T 세포치료제 7종과 고형암을 표적으로 하는 1종의 TCR-T가 있다(표 1).
이러한 유전자면역세포치료제는 2017년 최초로 FDA 허가받은 CAR-T 세포치료제 ‘Kymriah(Novartis社)’의 효능이 입증된 후 시장 경쟁이 더욱 커지고 있다.
하지만 현재 개발된 면역세포치료제는 유전자 도입 시에 생길 수 있는 삽입 돌연변이 유발(insertional mutagenesis), 사이토카인 방출 증후군(CRS, cytokine release syndrome) 및 신경독성 증후군(ICANS, immune effector cell-associated neurotoxicity syndrome)과 같은 심각한 부작용, 표적 항원 손실로 인한 내성, 항원이 발현되는 정상 조직을 함께 공격하는 문제점(on-target off-toxicity), 종양 미세환경으로 인한 고형암에서의 효능 및 지속성 저하 등 여러 한계점을 갖고 있다.
또한, 높은 효능에도 불구하고 환자 자가 세포를 이용한다는 점에서 복잡한 생산 공정에 따른 고가의 비용, 특정 환자 내 제작 어려움, 긴 제조 공정에 따른 환자 상태 악화 등 자가세포치료제로서의 개발 한계도 뒤따르고 있다.
따라서 최근 이러한 면역세포치료제의 한계점을 극복하면서도 높은 치료 유효성을 나타낼 수 있도록 유전자가위 기반의 유전자 편집 기술을 도입한 다양한 연구들이 진행되고 있다.
CRISPR 시스템을 이용한 면역 체크포인트 유전자 및 면역 억제 유전자 knock-out, epigenetic modification 조절 등의 유전자 편집 기술과 DNA base editing, CRISPR interference(CRISPRi), CRISPR activation(CRISPRa), prime editing 기반 유전자 제어 기술 등이 그것이다.
고형암의 면역 억제성, 종양 미세환경으로 인한 낮은 지속성과 치료 효능을 극복하고 부작용을 제어한 치료제뿐 아니라 광범위한 환자에 적용될 수 있도록 off-the-shelf(기성품) 치료제를 개발해 고가의 치료비용 문제를 해결하려는 시도도 이루어지고 있다.
본 기고문에서는 지속성과 효능을 높인 면역세포치료제 개발과 off-the-shelf 생산이 가능한 T세포 및 NK세포 등의 범용성 면역세포치료제 개발에서 이용되고 있는 유전자 편집 기술 및 관련 연구 동향을 살펴보고, 향후 개발의 방향성을 예상해보고자 한다.
표 1. FDA 승인된 유전자면역세포치료제 출처: FDA
2. 면역세포치료제 개발의 현재 동향
항암면역세포치료제는 앞서 언급한 바와 같이 환자 자가 또는 동종 면역세포를 활성화하거나 조작하여 암세포를 공격하도록 하는 치료법으로, 기존 화학요법 및 방사선 치료의 부작용인 정상세포 손상을 줄이는 표적 항암제로 작용하며 장기간의 면역 효과를 보일 수 있는 등의 다양한 장점을 갖고 있다. 이러한 면역세포치료제들 중 유전자가 도입된 대표적인 유형들은 다음과 같다.
● CAR-T(Chimeric Antigen Receptor-T cell) 치료: 환자의 T세포 내 CAR 유전자를 도입하여 암세포 특정 항원을 인식하고 공격하도록 만든 자가세포치료제
● CAR-NK 치료: 선천성 NK세포 내 CAR 유전자를 도입해 암세포를 효과적으로 치료하는 치료제로 주로 범용성 세포치료제로 개발
● CAR-γδT 세포 치료: 감마델타 T세포의 선천면역 및 적응면역 기능을 활용해 다양한 암세포를 공격하는 치료제
● CAR-Macrophage 치료: 대식세포에 CAR 유전자를 도입하여 암세포 탐식 및 제거 능력을 향상시키고 동시에 종양 미세환경을 조절하는 치료제
● CAR-NKT(Natural Killer T cell) 치료: NKT 세포에 CAR 유전자를 도입하여 NK와 T세포의 특성을 결합해 강력한 항암 효과를 유도하는 치료제
외부 유전자가 도입된 면역세포치료제는 앞서 언급한 것처럼 백혈병 및 림프종, 골수종을 표적으로 하는 CAR-T 세포치료제 7종 및 고형암을 표적으로 하는 1종의 TCR-T 등, 총 8종이 FDA로부터 승인된 바 있다.
또, 최근 국내에서도 CD19+ 림프종 표적 ‘안발셀(큐로셀 社, 임상 2상 완료)’, CD19+ 미만성 거대 B세포 림프종 표적 ‘AT-101(앱클론 社, 임상 2상)’, 재발성/불응성 B세포 비호지킨 림프종 표적 ‘TC011(티카로스 社, 임상 1/2a상)’, HER2+ 난소암 표적 ‘AT-501(앱클론 社, 전임상)’ 등의 개발이 이루어지고 있다.
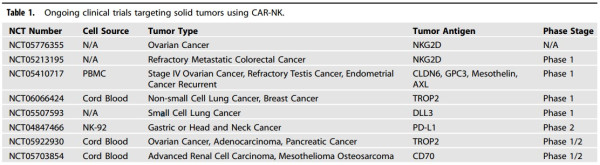
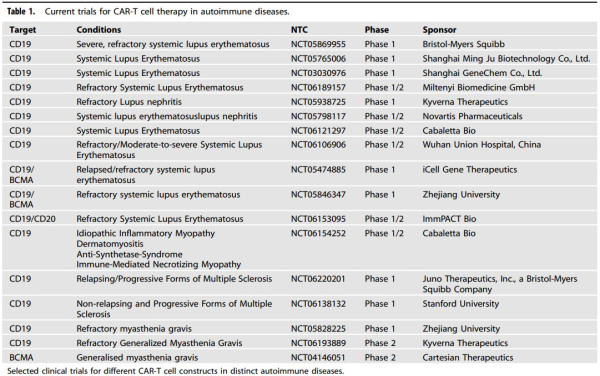
T세포 이외에도 범용성 세포치료제 개발이 가능한 NK세포를 기반으로 한 임상들도 활발히 진행되고 있다. 특히 고형암을 표적하는 NK 세포치료제(표 2) 및 자가면역질환 치료제(표 3) 등은 국외에서도 다수의 임상들이 진행 중이다. 최근에는 감염성 질환과 노화 관련 질환으로 적응증의 범위를 확장하여 개발하려는 시도들도 이루어지고 있다.
표 2. 고형암 표적 CAR-NK 세포치료제
표 3. 자가면역질환 표적 CAR-T 세포치료제
3. 면역세포치료에서 유전자 편집 기술의 역할
최근 면역세포치료제에 적용되는 유전자 편집 기술은 대표적으로 CRISPR 시스템을 이용한 유전자 Knock-out, Knock-in 등의 유전자 편집 기술과 Epigenetic modification 조절, dCas9을 이용한 CRISPRi, CRISPRa 유전자 제어 기술, 그리고 Base editing 및 Prime editing 등이 있다.
● CRISPR Knock-out, Knock-in: Cas9이 표적 DNA를 절단한 후 세포의 DNA 복구 기전을 이용해 유전자를 제거(Knock-out)하거나 삽입(Knock-in)
● Epigenetic Modification: CRISPR를 이용하여 DNA 메틸화, 히스톤 변형 관련 유전자를 조절하여 특정 유전자의 발현을 활성화하거나 억제
● dCas를 이용한 CRISPRi, CRISPRa: 활성을 제거한 dCas가 전사 억제 인자(CRISPRi) 또는 전사 활성 인자(CRISPRa)와 결합하여 특정 유전자의 발현을 조절
● Base Editing : 변형된 Cas9 단백질에 cytidine deaminase 또는 adenine deaminase 효소를 결합하여 DNA 이중가닥 절단(DSB, double strand break) 없이 특정 염기를 정밀하게 치환
● Prime Editing : 변형된 Cas9 단백질이 DNA 한 가닥만 절단하고 동시에 역전사효소(RT, reverse transcriptase)가 새로운 유전자 서열을 합성하여 원하는 변이를 삽입, 삭제, 또는 치환하는 방식
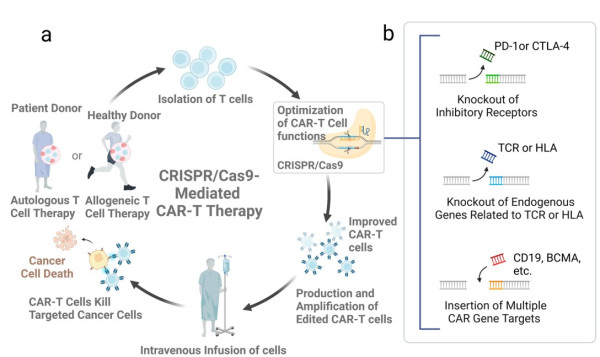
앞서 언급한 문제점을 해결하고자 면역세포치료제 개발 과정에 유전자 편집 기술을 적용함에 있어, 1) 면역조절 유전자 스크리닝, 2) 면역세포의 기능, 지속성 및 종양 사멸 능력을 높이기 위한 면역세포 유전자 엔지니어링, 3) 독성을 감소시키고 면역 과활성화 및 오프타겟 효과를 최소화하기 위한 유전자 편집, 4) 범용 Off-the-shelf 세포 제작을 통해 유전자 편집 기술 적용 동종이식(기증자 유래) 치료법 개발 및 환자 특이적 세포에 대한 의존도를 줄이는 시도들이 이루어지고 있다(그림1).
그림 1. 면역세포치료제 개발 과정에서 CRISPR 시스템의 이용
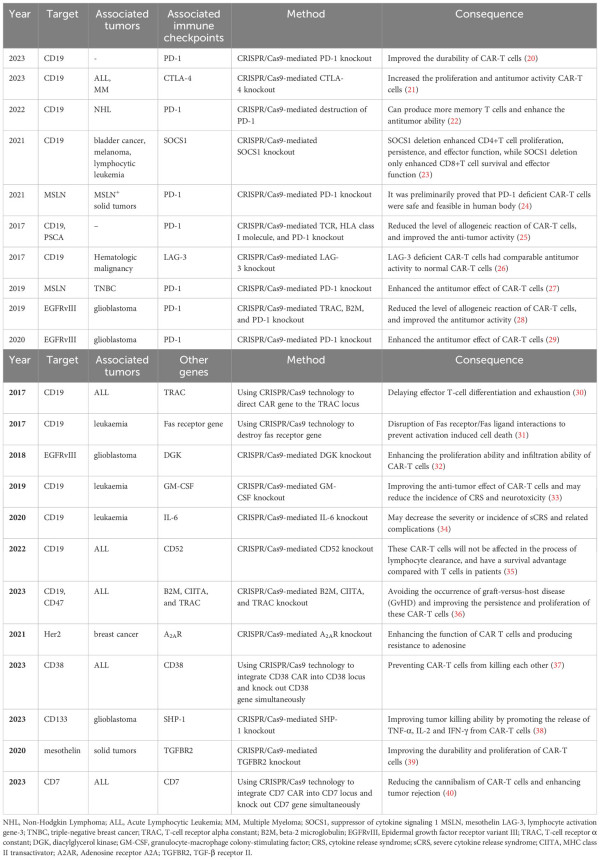
CAR 세포치료제의 효능을 높이기 위해 PD-1, CTLA4와 같은 면역 체크포인트 유전자를 Knock-out시키는 유전자 편집 연구들도 진행되고 있다(표 4).
표 4. 면역 체크포인트 유전자 편집 세포치료제
종양의 면역회피 기전을 무력화하기 위해 TGFβ 수용체 유전자를 Knock-out시킨 EGFR CAR-T, HPK1 유전자를 Knock-out시킨 XYF19 CAR-T 연구들 역시 성공적으로 임상 1상을 진행 중이다.
특히 범용 Off-the-shelf 세포 제작은 가장 활발하게 연구되고 있는 분야 중 하나다.
iPSC 유래 CD19 표적 CAR-NK 면역세포치료제 ‘FT596(FATE 社)’는 ‘rituximab’과 병용치료시 고무적인 효과를 보인다는 임상1상 결과가 발표된 바 있다.
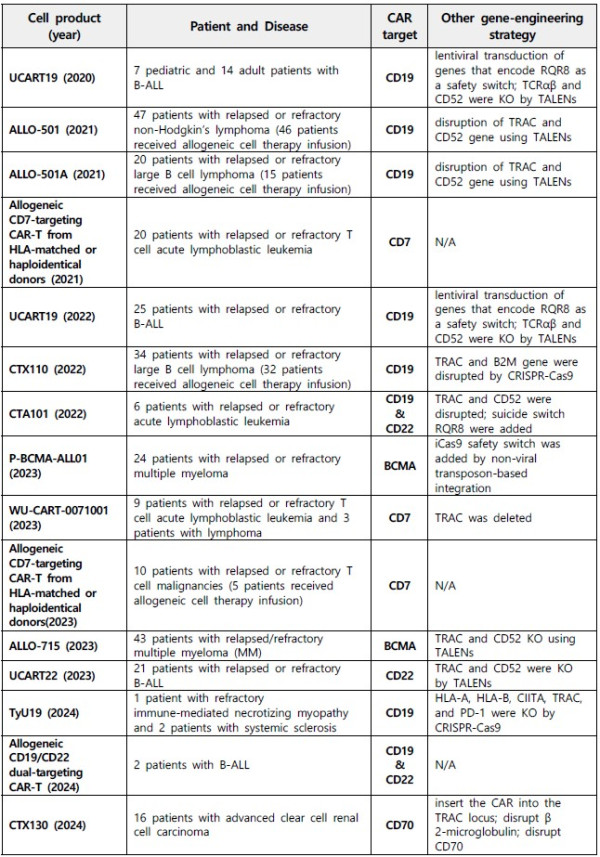
CRISPR 유전자 편집 기술을 이용한 Off-the-shelf CAR-T 또한 다수의 임상연구가 진행되고 있다(표5).
지난해에는 중국 칭화대학 연구팀이 HLA-A, HLA-B, CIITA, TRAC, PD-1 유전자를 Knock-out시킨 CD19 CAR-T인 ‘TyU19’를 투여한 환자들에서 CRS와 GvHD(graft versus host disease, 이식편대숙주병) 관련 증상이 나타나지 않았다는 임상연구 결과를 공개했다.
CAR 유전자를 TRAC locus에 발현시키고 β2 microglobulin과 CD70 유전자를 Knock-out시킨 CD70 CAR-T인 ‘CTX130(CRISPR 社’) 역시 임상 1상에 참여한 모든 환자들이 용량제한 독성(dose limiting toxicity)을 나타내지 않았다는 임상연구도 발표됐다. 연구팀은 피험자들의 질병조절율(dose control rate)은 81.3%에 육박한다고 밝히기도 했다.
표 5. Off-the-Shelf CAR-T 세포치료제
4. 미래 전망 및 결론
현재 다양한 질환을 표적으로, CRISPR 유전자 편집 기술을 접목시킨 면역세포치료제 상용화 연구는 이미 상당 부분 개발이 진행된 상태다.
초기 연구에서는 표적 암세포를 공격하는 기능을 확인하는 데 집중했다면, 최근의 연구 동향은 유전자 편집 기술을 적용해 기존의 한계를 극복하고 자가면역질환, 감염성 질환, 노화 관련 질환 등으로 표적 질환을 확장하는 데 많은 관심이 모아지고 있다.
다만 이러한 유전자 편집 기술 응용 면역세포치료제 개발에 있어서 제조 공정 및 비용 문제, 규제, 독성 문제, 특허 이슈 등은 해결해야 할 과제로 남아 있다.
그럼에도 불구하고 유전자 편집 기술은 미래 의료 산업의 주요 축으로 부상할만한 잠재력을 갖고 있으며, 면역세포치료제의 효능 개선 및 단점 극복을 위한 하나의 ‘킥(kick)’임은 분명하다.
기존의 한계를 극복해 암 치료 이상의 혁신적인 치료제를 탄생시키고 지속적으로 발전시키는 데 있어 두 기술의 융합이 시너지 효과를 낼 것으로 사료된다.
* 본 기고문은 과학기술정보통신부에서 시행한 「유전자편집·제어·복원기반기술개발사업」수행의 일환으로 작성되었습니다.
* 본 내용은 유전체편집연구지원사무국(GERC)의 의견과 다를 수 있음을 밝힙니다.
* 인용, 발표하실 때에는 반드시 출처를 밝혀주시기 바랍니다.